1. Definición
Es el estudio de las sustancias, especialmente de su estructura, composición, propiedades y transformaciones.
2. El papel de la química en la vida cotidiana
El conocimiento de la química ha beneficiado de muchas maneras. Se han podido desarrollar los plásticos y los polímeros, que ahora se utilizan en casi todos los aspectos de la vida, se han descubierto sustancias farmacéuticas que mejoran la salud y prolongan la vida. Se ha incrementado la producción de alimentos al desarrollar fertilizantes y pesticidas. Se han aprendido a utilizar los productos de procesos químicos que se efectúan naturalmente, como el petróleo y el carbón, para proporcionar la energía, y las materias primas que hacen posible nuestra moderna forma de vida.
3. Ramas de la química y sus aplicaciones
a) Química orgánica: La química de la mayoría de los compuestos del carbono.
b) Química inorgánica: La química de todos los elementos excepto el carbono. Algunos compuestos de carbono sencillos (dióxidos de carbono y carbonatos) están tradicionalmente clasificados como compuestos inorgánicos.
c) Química analítica: Trata de la identificación y de la composición tanto cualitativa como cuantitativa de las sustancias.
d) Fisicoquímica: Tiene que ver con el estudio de los principios físicos que rigen la estructura de la materia y las transformaciones químicas.
e) Bioquímica: Es la química de los sistemas vivos, plantas y animales.
4. La química y su relación con otras ciencias
a) Matemáticas.- Las matemáticas consituyen una herramienta esencial en la cuantificación de los fenómenos químicos (desde la estequiometría de las reacciones hasta el cálculo de los tiempos de vida media de los elementos radiactivos).
b) Con la Física. Dando orígen a la "Fisicoquímica" que es la disciplina que estudia fenómenos como los cambios de fase en la materia, termodinámica y cinética de reacciones químicas, química coloidal, electroquímica, etc.
c) Con la Biología. Dando origen a la Bioquímica que es la disciplina que estudia los fenómenos ocurridos en los seres vivos a nivel molecular. Desde la composicion de la materia viviente hasta los complejos procesos metabólicos que se presentan en todo ser vivo.
5. La química y su relación con el medio ambiente
Los beneficios que la química ha proporcionado no han venido sin tener que pagar un precio. Cada vez más, encontramos que la dependencia de la química ha originado daños ambientales, inesperados problemas de salud y tragedias humanas, como el envenenamiento de los peces en el mar cerca de una planta química en Japón en 1971 y que provocó deformaciones de la gente por envenenamiento con mercurio o la fuga de sustancias tóxicas en Bhopal, India, en 1984 que mató o causó daños a más de 40,000 personas.
5.1 Contaminación de los recurso naturales y sus efectos
5.1.1 Lluvia ácida
La lluvia tiene un pH igual a 5.6. Esto se debe a que, en su viaje desde las nubes hasta la superficie terrestre, el agua de la lluvia disuelve parte del CO2 de la atmósfera y forma ácido carbónico (H2CO3), que es un ácido débil: Si la atmósfera está contaminadas por óxidos de azufre y de nitrógeno, se producen los ácidos sulfúrico (H2SO4), nitroso (HNO2) y nítrico (HNO3).
Si la atmósfera está contaminadas por óxidos de azufre y de nitrógeno, se producen los ácidos sulfúrico (H2SO4), nitroso (HNO2) y nítrico (HNO3).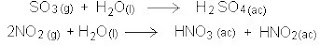 La lluvia contaminada con estos ácidos se conoce como lluvia ácida y llega a alcanzar una acidez cercana a un pH 3.0. La precipitación ácida provoca que las estructuras metálicas se corroan, que la fotosíntesis se realice lentamente, que mueran plantas y, por supuesto, los peces de lagos y ríos. En ocasiones, los lagos tienen suelos con gran cantidad de carbonatos; estos compuestos reaccionan con la lluvia ácida y la neutralizan de acuerdo a la siguiente reacción:
La lluvia contaminada con estos ácidos se conoce como lluvia ácida y llega a alcanzar una acidez cercana a un pH 3.0. La precipitación ácida provoca que las estructuras metálicas se corroan, que la fotosíntesis se realice lentamente, que mueran plantas y, por supuesto, los peces de lagos y ríos. En ocasiones, los lagos tienen suelos con gran cantidad de carbonatos; estos compuestos reaccionan con la lluvia ácida y la neutralizan de acuerdo a la siguiente reacción: 5.1.2 Ozono
5.1.2 Ozono
EL El ozono es un gas cuyas moléculas están formadas por tres átomos de oxígeno(O3), uno más que las moléculas de oxígeno que respiramos. La capa de ozono se fue engrosando a medida que fue aumentando la cantidad de oxígeno. Esto es así porque su formación se debe a reacciones químicas entre el oxígeno y los rayos ultravioletas.
En efecto, la capa de ozono es para los seres vivos un protector frente a los peligrosísimos rayos ultravioletas.
En 1974, dos científicos estadounidenses Sherwood Rowland y Mario Molina descubrieron que los CFC (Compuestos Fluorocarbonados), sustancias muy utilizadas en la industria, destruyen el ozono.
Rowland y Molina fueron atacados por las empresas productoras, pero pocos años después se detectó que con la llegada de la primavera, el espesor de la capa de ozono sobre la Antártida era anormalmente delgado y se comprobó que la causa era el uso de CFC. En 1987, 40 países industrializados pactaron en Montreal la reducción de la producción de CFC en un 50% en el año 2000.
5.1.3 Efecto invernadero
Efecto invernadero, se está produciendo un incremento del contenido en anhídrido carbónico en la atmósfera a causa de la quema indiscriminada de combustibles fósiles, como el carbón y la gasolina, y de la destrucción de los bosques tropicales.
Consecuencias:
*Aumento de la temperatura media del planeta.
*Aumento de sequías en unas zonas e inundaciones en otras.
*Mayor frecuencia de formación de huracanes.
* Progresivo deshielo de los casquetes polares, con la consiguiente subida de los niveles de los océanos.
*Incremento de las precipitaciones a nivel planetario pero lloverá menos días y más torrencialmente.
5.1.4 Metales pesados
El término "metal pesado" no está bien definido. A veces se emplea el criterio de densidad. Por ejemplo, metales de densidad mayor que 4,5 g/cm³, pero los valores en la bibliografía pueden ir desde 4 g/cm³ hasta 7 g/cm³.
Mercurio: La exposición al nivel local del Mercurio ocasiona irritación de la piel, mucosa y es sensibilizante de la piel. En casos de exposición a altas dosis en forma oral, colapsa el aparato digestivo, siendo mortal en horas.
Cadmio: Las fuentes más comunes son las pilas, -qué también contienen Mercurio-, los pigmentos para pinturas, los barnices y las cañerías de PVC. Este metal es sumamente tóxico, además de cancerígeno. En madres expuestas al Cadmio produce serias afecciones con lesiones para el embarazo, presencia de proteína en la orina, etc.
Plomo: Síntomas avanzados: anemia, cólicos intestinales, nauseas y vómitos, enfermedad renal, impotencia sexual, delirio, esterilidad, daños al feto, hipertensión arterial, estreñimiento agudo, afectación de los nervios, enfermedad o sea, problemas de cáncer y MUERTE...
Cromo: Afecciones locales: sobre la piel causan dermatitis, sensibilización de la piel, es irritante de la piel y mucosas Afecciones generales: produce tos, bronquitis crónica, ulceraciones del tabique nasal y piel, dolores respiratorios y de cabeza, hemorragia nasal, dermatitis, etc.
Zinc, Manganeso, Cobre, Bismuto, Plata y Níquel: son también sustancias tóxicas, que producen de las más diversas alteraciones a la salud humana.
5.1.5 Plaguicidas
La contaminación del agua por plaguicidas se produce al ser arrastrados por el agua de los campos de cultivo hasta los ríos y mares donde se introducen en las cadenas alimenticias provocando la muerte de varias formas de vida necesarias en el balance de algunos ecosistemas. Estos compuestos químicos han provocado la muerte de peces tanto en agua dulce como salada, también se acumulan en los tejidos de algunos peces los que a su vez ponen en peligro la vida de sus consumidores. Los plaguicidas acumulados en las aguas ponen en peligro la vida de animales y vegetales acuáticos. En condiciones de laboratorio se ha observado que algunos de ellos son cancerígenos, teratogénicos y mutágenos en ratas, hamsters y monos.
5.1.6 Detergentes
La mayoría de los detergentes sintéticos son contaminantes persistentes debido a que no son descompuestos fácilmente por la acción bacteriana. A los detergentes que no son biodegradables se les llama detergentes duros y a los degradables, detergentes blandos.
El principal agente tensoactivo que se usa en los detergentes es un derivado del alquilbencensulfonato como, por ejemplo, el dodecilbencensulfonato de sodio el cual puede hacer al detergente duro (no biodegradable, contaminante persistente) o blando (biodegradable, contaminante biodegradable), dependiendo del tipo de ramificaciones que tenga.
5.1.7 Radioactividad
La contaminación radiactiva es producida principalmente por el uso de sustancias radiactivas naturales o artificiales, el uso de la energía nuclear y de la invensión de la bomba atómica ha llegado a constituir un gran peligro de contaminación para la naturaleza y la humanidad; ya que se han esparcido por toda la tierra muchos residuos de los materiales contaminantes que se usan para realizar las pruebas nucleares, asi como los residuos que quedan tambien en el agua que se usa para enfriar los reactores.
Es el estudio de las sustancias, especialmente de su estructura, composición, propiedades y transformaciones.
2. El papel de la química en la vida cotidiana
El conocimiento de la química ha beneficiado de muchas maneras. Se han podido desarrollar los plásticos y los polímeros, que ahora se utilizan en casi todos los aspectos de la vida, se han descubierto sustancias farmacéuticas que mejoran la salud y prolongan la vida. Se ha incrementado la producción de alimentos al desarrollar fertilizantes y pesticidas. Se han aprendido a utilizar los productos de procesos químicos que se efectúan naturalmente, como el petróleo y el carbón, para proporcionar la energía, y las materias primas que hacen posible nuestra moderna forma de vida.
3. Ramas de la química y sus aplicaciones
a) Química orgánica: La química de la mayoría de los compuestos del carbono.
b) Química inorgánica: La química de todos los elementos excepto el carbono. Algunos compuestos de carbono sencillos (dióxidos de carbono y carbonatos) están tradicionalmente clasificados como compuestos inorgánicos.
c) Química analítica: Trata de la identificación y de la composición tanto cualitativa como cuantitativa de las sustancias.
d) Fisicoquímica: Tiene que ver con el estudio de los principios físicos que rigen la estructura de la materia y las transformaciones químicas.
e) Bioquímica: Es la química de los sistemas vivos, plantas y animales.
4. La química y su relación con otras ciencias
a) Matemáticas.- Las matemáticas consituyen una herramienta esencial en la cuantificación de los fenómenos químicos (desde la estequiometría de las reacciones hasta el cálculo de los tiempos de vida media de los elementos radiactivos).
b) Con la Física. Dando orígen a la "Fisicoquímica" que es la disciplina que estudia fenómenos como los cambios de fase en la materia, termodinámica y cinética de reacciones químicas, química coloidal, electroquímica, etc.
c) Con la Biología. Dando origen a la Bioquímica que es la disciplina que estudia los fenómenos ocurridos en los seres vivos a nivel molecular. Desde la composicion de la materia viviente hasta los complejos procesos metabólicos que se presentan en todo ser vivo.
5. La química y su relación con el medio ambiente
Los beneficios que la química ha proporcionado no han venido sin tener que pagar un precio. Cada vez más, encontramos que la dependencia de la química ha originado daños ambientales, inesperados problemas de salud y tragedias humanas, como el envenenamiento de los peces en el mar cerca de una planta química en Japón en 1971 y que provocó deformaciones de la gente por envenenamiento con mercurio o la fuga de sustancias tóxicas en Bhopal, India, en 1984 que mató o causó daños a más de 40,000 personas.
5.1 Contaminación de los recurso naturales y sus efectos
5.1.1 Lluvia ácida
La lluvia tiene un pH igual a 5.6. Esto se debe a que, en su viaje desde las nubes hasta la superficie terrestre, el agua de la lluvia disuelve parte del CO2 de la atmósfera y forma ácido carbónico (H2CO3), que es un ácido débil:
 Si la atmósfera está contaminadas por óxidos de azufre y de nitrógeno, se producen los ácidos sulfúrico (H2SO4), nitroso (HNO2) y nítrico (HNO3).
Si la atmósfera está contaminadas por óxidos de azufre y de nitrógeno, se producen los ácidos sulfúrico (H2SO4), nitroso (HNO2) y nítrico (HNO3).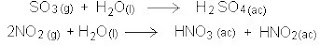 La lluvia contaminada con estos ácidos se conoce como lluvia ácida y llega a alcanzar una acidez cercana a un pH 3.0. La precipitación ácida provoca que las estructuras metálicas se corroan, que la fotosíntesis se realice lentamente, que mueran plantas y, por supuesto, los peces de lagos y ríos. En ocasiones, los lagos tienen suelos con gran cantidad de carbonatos; estos compuestos reaccionan con la lluvia ácida y la neutralizan de acuerdo a la siguiente reacción:
La lluvia contaminada con estos ácidos se conoce como lluvia ácida y llega a alcanzar una acidez cercana a un pH 3.0. La precipitación ácida provoca que las estructuras metálicas se corroan, que la fotosíntesis se realice lentamente, que mueran plantas y, por supuesto, los peces de lagos y ríos. En ocasiones, los lagos tienen suelos con gran cantidad de carbonatos; estos compuestos reaccionan con la lluvia ácida y la neutralizan de acuerdo a la siguiente reacción: 5.1.2 Ozono
5.1.2 OzonoEL El ozono es un gas cuyas moléculas están formadas por tres átomos de oxígeno(O3), uno más que las moléculas de oxígeno que respiramos. La capa de ozono se fue engrosando a medida que fue aumentando la cantidad de oxígeno. Esto es así porque su formación se debe a reacciones químicas entre el oxígeno y los rayos ultravioletas.
En efecto, la capa de ozono es para los seres vivos un protector frente a los peligrosísimos rayos ultravioletas.
En 1974, dos científicos estadounidenses Sherwood Rowland y Mario Molina descubrieron que los CFC (Compuestos Fluorocarbonados), sustancias muy utilizadas en la industria, destruyen el ozono.
Rowland y Molina fueron atacados por las empresas productoras, pero pocos años después se detectó que con la llegada de la primavera, el espesor de la capa de ozono sobre la Antártida era anormalmente delgado y se comprobó que la causa era el uso de CFC. En 1987, 40 países industrializados pactaron en Montreal la reducción de la producción de CFC en un 50% en el año 2000.
5.1.3 Efecto invernadero
Efecto invernadero, se está produciendo un incremento del contenido en anhídrido carbónico en la atmósfera a causa de la quema indiscriminada de combustibles fósiles, como el carbón y la gasolina, y de la destrucción de los bosques tropicales.
Consecuencias:
*Aumento de la temperatura media del planeta.
*Aumento de sequías en unas zonas e inundaciones en otras.
*Mayor frecuencia de formación de huracanes.
* Progresivo deshielo de los casquetes polares, con la consiguiente subida de los niveles de los océanos.
*Incremento de las precipitaciones a nivel planetario pero lloverá menos días y más torrencialmente.
5.1.4 Metales pesados
El término "metal pesado" no está bien definido. A veces se emplea el criterio de densidad. Por ejemplo, metales de densidad mayor que 4,5 g/cm³, pero los valores en la bibliografía pueden ir desde 4 g/cm³ hasta 7 g/cm³.
Mercurio: La exposición al nivel local del Mercurio ocasiona irritación de la piel, mucosa y es sensibilizante de la piel. En casos de exposición a altas dosis en forma oral, colapsa el aparato digestivo, siendo mortal en horas.
Cadmio: Las fuentes más comunes son las pilas, -qué también contienen Mercurio-, los pigmentos para pinturas, los barnices y las cañerías de PVC. Este metal es sumamente tóxico, además de cancerígeno. En madres expuestas al Cadmio produce serias afecciones con lesiones para el embarazo, presencia de proteína en la orina, etc.
Plomo: Síntomas avanzados: anemia, cólicos intestinales, nauseas y vómitos, enfermedad renal, impotencia sexual, delirio, esterilidad, daños al feto, hipertensión arterial, estreñimiento agudo, afectación de los nervios, enfermedad o sea, problemas de cáncer y MUERTE...
Cromo: Afecciones locales: sobre la piel causan dermatitis, sensibilización de la piel, es irritante de la piel y mucosas Afecciones generales: produce tos, bronquitis crónica, ulceraciones del tabique nasal y piel, dolores respiratorios y de cabeza, hemorragia nasal, dermatitis, etc.
Zinc, Manganeso, Cobre, Bismuto, Plata y Níquel: son también sustancias tóxicas, que producen de las más diversas alteraciones a la salud humana.
5.1.5 Plaguicidas
La contaminación del agua por plaguicidas se produce al ser arrastrados por el agua de los campos de cultivo hasta los ríos y mares donde se introducen en las cadenas alimenticias provocando la muerte de varias formas de vida necesarias en el balance de algunos ecosistemas. Estos compuestos químicos han provocado la muerte de peces tanto en agua dulce como salada, también se acumulan en los tejidos de algunos peces los que a su vez ponen en peligro la vida de sus consumidores. Los plaguicidas acumulados en las aguas ponen en peligro la vida de animales y vegetales acuáticos. En condiciones de laboratorio se ha observado que algunos de ellos son cancerígenos, teratogénicos y mutágenos en ratas, hamsters y monos.
5.1.6 Detergentes
La mayoría de los detergentes sintéticos son contaminantes persistentes debido a que no son descompuestos fácilmente por la acción bacteriana. A los detergentes que no son biodegradables se les llama detergentes duros y a los degradables, detergentes blandos.
El principal agente tensoactivo que se usa en los detergentes es un derivado del alquilbencensulfonato como, por ejemplo, el dodecilbencensulfonato de sodio el cual puede hacer al detergente duro (no biodegradable, contaminante persistente) o blando (biodegradable, contaminante biodegradable), dependiendo del tipo de ramificaciones que tenga.
5.1.7 Radioactividad
La contaminación radiactiva es producida principalmente por el uso de sustancias radiactivas naturales o artificiales, el uso de la energía nuclear y de la invensión de la bomba atómica ha llegado a constituir un gran peligro de contaminación para la naturaleza y la humanidad; ya que se han esparcido por toda la tierra muchos residuos de los materiales contaminantes que se usan para realizar las pruebas nucleares, asi como los residuos que quedan tambien en el agua que se usa para enfriar los reactores.
Comentarios
Solo quiero decirle que esta pagina es muy interesante y practica, para muchos o al menos para mi se me hace mas facil bajar la informacion directamente de aqui espero podermela llevar bien con usted. Soy una de sus alumnas del propedeutico.